近日,药物所汪小涧团队联合清华大学自动化系脑与认知科学研究所季向阳团队在《Nature communications》在线发表题为“RSGPT: a generative transformer model for retrosynthesis planning pre-trained on ten billion datapoints”的研究论文,成功构建了基于大规模预训练的逆合成规划模型RSGPT:借助RDChial算法匹配化学反应模板生成百亿化学反应数据,并引入了RLAIF策略优化预测反应原料的合理性,最终实现了RSGPT模型在合成推断任务上的SOTA水平,为智能合成规划研究提供了新范式。
近年来,汪小涧团队聚焦于生成式AI在药物发现领域的应用与研究,系统性地开展了一系列前沿探索。在药物分子设计(Brief. Bioinform. 2023),基于碳谱的结构解析 (Anal. Chem. 2021; Anal. Chem. 2023; Anal. Chem. 2024) ,合成路径规划 (Chin. Chem. Lett. 2025, 10.1016/j.cclet.2025.110968)等领域取得了多项重要研究成果。
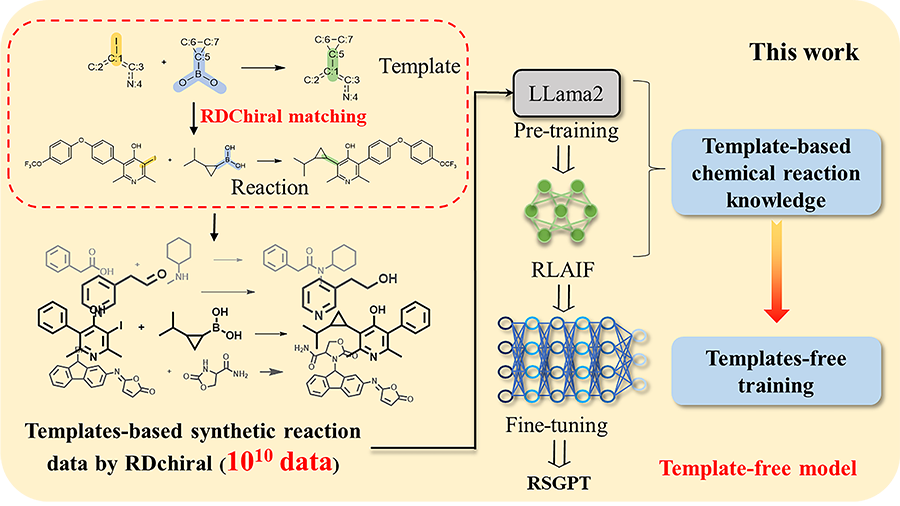
在前期研究工作的基础上,研究团队针对逆合成规划领域缺少高质量数据的焦点,创新性地采用RDChiral逆向模板提取算法,基于PubChem等数据库的分子,通过精准匹配反应中心生成百亿余化学反应数据。该数据构建策略不仅全面涵盖了现有的化学反应空间,更拓展至传统数据集未曾触及的未知区域。通过这种预训练机制,模型能够自发性地捕捉和理解复杂的化学反应规律。
基于上述合成数据,我们成功构建了基于LLaMA2架构的生成式预训练模型RSGPT,并结合人工智能反馈强化学习(RLAIF)机制。通过RDChiral这一专业软件验证生成物与模板的化学合理性,最终实现了模型在无模板输入的情况下仍能精确预测反应物。该模型在USPTO-50k基准测试中Top-1准确率达63.4%,显著超越现有所有其他智能合成规划方法,为复杂有机分子合成提供了智能化解决方案。
药物所汪小涧研究员、清华大学季向阳教授为本文共同通讯作者,清华大学邓亚峰博士、赵信达与药物所孙涵宇博士为本文共同第一作者。本研究工作在开展过程中获得了药物所李广研究员的重要支持与指导,得到了国家自然科学基金(82373718)、中国医学科学院医学与健康科技创新工程(2021-1-2M-028)及澳门科学技术发展基金(No.006/2023/SKL)的资助。
论文链接:https://www.nature.com/articles/s41467-025-62308-6