近日,药物所张天泰团队在国际知名期刊《Bioactive Materials》在线发表了题为“Immunomodulatory supramolecular hydrogel for rheumatoid arthritis management via adenosine A2A receptor-mediated macrophage remodeling”的研究论文。该研究成功开发了一种可注射超分子水凝胶系统(PNSH@MTX),通过席夫碱反应交联葡甘聚糖与负载甲氨蝶呤的纳米粒(mPECN-MTX NPs),旨在实现药物的长效缓控释放,并精准靶向巨噬细胞重塑炎性微环境,从而有效抑制类风湿关节炎(RA)疾病进展。
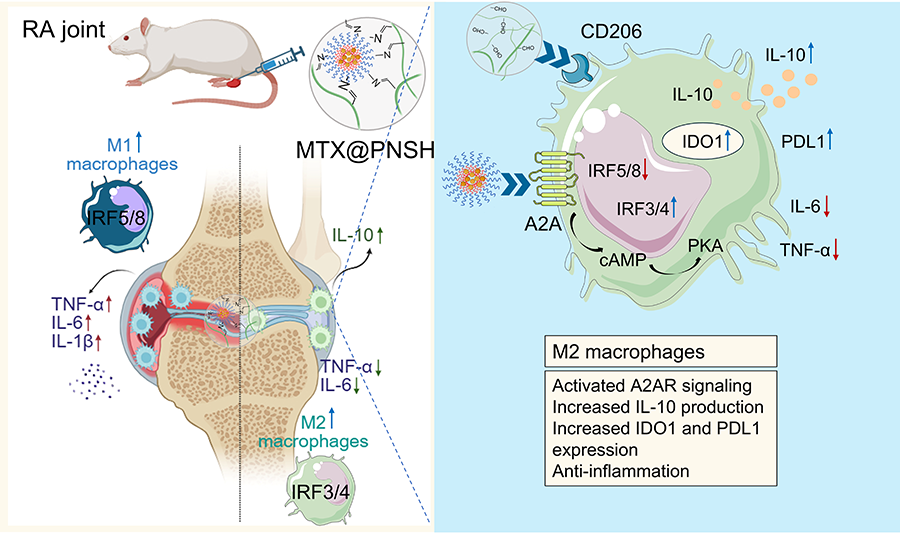
在RA发病过程中,关节腔内促炎巨噬细胞长期浸润导致的免疫微环境失衡是滑膜炎症、关节损伤和功能障碍的关键因素,甲氨蝶呤(MTX)是目前RA治疗的一线药物,但口服给药存在多种副作用。研究团队设计并构建了一种具有动态力学性能和形态的PNSH@MTX,具有可注射和酸敏感的特点。在关节腔内,mPECN-MTX NPs表面修饰的氧化葡甘聚糖通过识别甘露糖受体(MR)精准靶向炎性巨噬细胞,并缓慢释放MTX,低剂量MTX通过上调胞外嘌呤信号通路的关键分子CD39、CD73,特异性激活巨噬细胞上的A2AR受体,启动IDO1-PDL1免疫代谢途径,进而促进M2型巨噬细胞相关转录因子IRF3/4的表达,并显著下调M1型巨噬细胞相关转录因子IRF5/8,从而使关节腔内炎性巨噬细胞重编程为M2型巨噬细胞。结果表明,PNSH@MTX在关节腔内重塑了炎症与免疫微环境,并降低了MTX的系统毒性,在调控炎症和治疗RA方面展现出了较大应用潜力,为RA的精准免疫治疗提供了新策略。
药物所史高娜副研究员、隗雅姿助理研究员、约翰霍普金斯大学博士后刘祥为本文共同第一作者,药物所张天泰研究员、孙岚研究员、南开大学王伟伟教授为本文共同通讯作者。该工作得到了中国医学科学院医学与健康科技创新工程(2024-I2M-ZH-010)、中央高校基本科研业务费(2024-JKCS-28)、国家自然科学基金(82273936,82293684)等项目的资助。
论文链接:https://doi.org/10.1016/j.bioactmat.2025.11.031